Soal 1
Perhatikan model atom berikut:
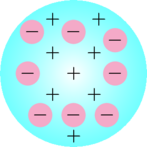
Model atom di atas dikemukakan oleh …
(A) Dalton
(B) Thomson
(C) Rutherford
(D) Bohr
(E) Pauli
Jawaban: B
Soal 2
Berikut pernyataan tentang model atom:
- Atom dimodelkan sebagai bola pejal yang bermuatan positif dengan elektron-elektron yang tersebar di dalamnya
- Atom terdiri dari partikel subatomik yaitu proton dan neutron yang membentuk inti atom dan elektron yang bergerak mengelilingi inti pada orbital-orbital tertentu yang membentuk kulit atom
- Elektron bergerak mengelilingi inti atom pada lintasan-lintasan dengan tingkat energi tertentu
- Elektron dapat berpindah lintasan dengan menyerap atau melepaskan energi
Model atom menurut Bohr adalah …
(A) 1 dan 3
(B) 1 dan 4
(C) 2 dan 3
(D) 2 dan 4
(E) 3 dan 4
Jawaban : E
Soal 3
Atom \(^{12}_{24}\ce {Mg}\) dapat membentuk ion \(\ce {Mg^{2+}}\). Pernyataan yang bernar untuk ion \(\ce {Mg^{2+}}\) adalah …
(A) Memiliki jumlah proton 12
(B) Memiliki jumlah neutron 36
(C) Memiliki jumlah elektron 22
(D) Jumlah protonnya sama dengan jumlah elektron
(E) Jumlah neutron sama dengan jumlah elektron
Jawaban : C
Atom magnesium melepaskan 2 buah elektron sehingga terbentuk ion \(\ce {Mg^{2+}}\). Jumlah elektron pada ion \(\ce {Mg^{2+}}\) adalah 24 − 2 = 22 elektron
Soal 4
Ion \(\ce {Br}^{-}\) memiliki konfigurasi elektron \([\text{Ar}]\:4\text{s}^2\:3\text{d}^{10}\:4\text{p}^6\). Jika atom bromin memiliki jumlah neutron 45, maka nomor massa atom bromin adalah …
(A) 70
(B) 72
(C) 75
(D) 78
(E) 80
Jawaban: E
Konfigurasi atom \(\ce {Br} : [\text{Ar}]\:4\text{s}^2\:3\text{d}^{10}\:4\text{p}^5\). Atom unsur bromin memiliki jumlah elektron 35, sehingga nomor atom bromin 35.
Nomor massa = nomor atom + neutron
Nomor massa = 35 + 45 = 80
Soal 5
Jika konfigurasi ion \(\text{S}^{2-}\) adalah \(1\text{s}^2\:2\text{s}^2\:2\text{p}^6\:3\text{s}^2\:3\text{p}^6\) maka nomor atom S adalah …
(A) 10
(B) 11
(C) 12
(D) 13
(E) 16
Jawaban : E
konfigurasi atom \(\text{S}\) adalah \(1\text{s}^2\:2\text{s}^2\:2\text{p}^6\:3\text{s}^2\:3\text{p}^4\)
Jumlah elektron atom sulfur ada sebanyak 16, sehingga nomor atom S adalah 16
Soal 6
Banyaknya elektron yang tidak berpasangan dalam atom \(_{24}\text{X}\) adalah …
(A) 4
(B) 5
(C) 6
(D) 7
(E) 8
Jawaban : C
Konfigurasi elektron atom \(_{24}\text{X} = [\text{Ar}] 4\text{s}^1 3\text{d}^5\)
\([\text{Ar}]\:\boxed{\uparrow\:}\:\boxed{\uparrow|\uparrow|\uparrow|\uparrow|\uparrow}\)
Banyaknya elektron yang tidak berpasangan dalam atom \(_{24}\text{X}\) ada 6
Soal 7
Konfigurasi elektron atom suatu unsur adalah \(1\text{s}^2\:2\text{s}^2\:2\text{p}^6\:3\text{s}^2\:3\text{p}^6\:4\text{s}^2\). Bilangan oksidasi tertinggi yang dapat dimiliki oleh unsur tersebut adalah …
(A) +1
(B) +2
(C) +3
(D) +4
(E) +5
Jawaban : B
Konfigurasi elektron atom unsur tersebut dapat ditulis dengan:
\([\text{Ar}]\:4\text{s}^2\)
Unsur tersebut terletak di golongan IIA, dengan bilangan oksidasi tertinggi +2
Soal 8
Berikut ini adalah deretan bilangan kuantum yang dimiliki oleh suatu elektron. Deretan bilangan kuantum yang tidak mungkin adalah …
(A) \(n = 2, \: l = 0; \: m = 0, \: s = -\frac{1}{2}\)
(B) \(n = 2, \: l = 1; \: m = -2, \: s = +\frac{1}{2}\)
(C) \(n = 3, \: l = 0; \: m = 0, \: s = +\frac{1}{2}\)
(D) \(n = 3, \: l = 1; \: m = + 1, \: s = +\frac{1}{2}\)
(E) \(n = 3, \: l = 1; \: m = + 1, \: s = -\frac{1}{2}\)
Jawaban: B
Bilangan kuantum yang dimiliki suatu elektron tidak mungkin:
\(n = 2, \: l = 1; \: m = -2, \: s = +\frac{1}{2}\)
Karena untuk \(l = 1\) nilai \(m\) adalah −1, 0, +1, jadi tidak mungkin \(m = -2\)
Soal 9
Pasangan unsur yang memiliki kemiripan sifat adalah …
(A) \(_{11}\text{A} \text{ dan } _{23}\text{B}\)
(B) \(_{12}\text{C} \text{ dan } _{24}\text{D}\)
(C) \(_{7}\text{E} \text{ dan } _{13}\text{F}\)
(D) \(_{9}\text{G} \text{ dan } _{17}\text{H}\)
(E) \(_{3}\text{I} \text{ dan } _{4}\text{J}\)
Jawaban : D
Unsur-unsur yang memiliki kemiripan sifat diletakkan dalam satu golongan yang sama.
\(_{9}\text{G} \text{ dan } _{17}\text{H}\) sama-sama terletak pada golongan VIIA
Soal 10
Atom suatu unsur dengan jumlah proton 20, mempunyai sifat yang mirip dengan atom suatu unsur yang mempunyai jumlah proton …
(A) 11
(B) 12
(C) 13
(D) 15
(E) 16
Jawaban : B
atom suatu unsur dengan jumlah proton 20 memiliki jumlah elektron yang sama dengan 20 juga.
Konfigurasi elektron unsur tersebut adalah: \([\text{Ar}]\:4\text{s}^2\) (terletak pada golongan IIA).
Unsur lain yang juga terletak pada golongan IIA adalah unsur dengan jumlah proton pada atomnya 12.
Soal 11
Berikut ini adalah pernyataan untuk unsur-unsur:
\(^{23}_{11}\text{A}, \:^{9}_{4}\text{B}, \:^{27}_{13}\text{C}, \:^{32}_{16}\text{D},\: ^{19}_{9}\text{E}, \:^{20}_{10}\text{F}\)
- Unsur A memiliki jari-jari atom terbesar
- Potensial ionisasi terkecil adalah F
- Unsur E lebih elektronegatif dari unsur C
- Unsur A, B, dan C adalah logam
- Unsur E termasuk dalam golongan gas mulia
Pernyataan yang benar tentang unsur-unsur tersebut ditunjukkan oleh nomor …
(A) 1, 2, dan 3
(B) 2, 3, dan 4
(C) 1, 3, dan 4
(D) 2, 3, dan 5
(E) 3, 4, dan 5
Jawaban: C
\(^{23}_{11}\text{A} : 2, 8, 1\: (\text{golongan IA periode 3})\)
\(^{9}_{4}\text{B} : 2, 2 \:(\text{golongan IIA periode 2})\)
\(^{27}_{13}\text{C} : 2, 8, 3 \:(\text{golongan IIIA periode 3})\)
\(^{32}_{16}\text{D} : 2, 8, 6 \:(\text{golongan VIA periode 3})\)
\(^{19}_{9}\text{E} : 2, 7 \:(\text{golongan VIIA periode 2})\)
\(^{20}_{10}\text{F} : 2, 8 \:(\text{golongan VIIIA periode 2})\)
Jari-jari terbesar unsur A
Potensial ionisasi terkecil adalah A
Unsur E lebih elektronegatif dari unsur C
Unsur A, B, dan C adalah logam
Unsur E termasuk dalam golongan halogen
Soal 12
Berikut ini adalah data keelektronegatifan unsur-unsur
\begin{array}{|c |c |c | }\hline \text{Unsur} & \text{K} & \text{L} & \text{M} & \text{N} & \text{O} & \text{P}\\ \text{keelektronegatifan} & 2,1 & 1,5 & 0,9 & 3,0 & 1,2 & 1,8\\ \hline \end{array}
Urutan unsur-unsur dari kiri ke kanan dalam satu periode adalah …
(A) O − P − N − L
(B) L − P − O − M
(C) M − O − P − N
(D) K − L − N − O
(E) L − N − O − P
Nilai keelektronegatifan unsur dalam satu periode dari kiri ke kanan semakin besar
Jadi, urutan unsur-unsur dari kiri ke kanan dalam satu periode yang benar adalah
M − O − P − N
Soal 13
Jika jari-jari atom Be, B, Li, Na, dan K secara acak adalah 0,89; 0,80; 1,23; 1,57; 2,01 (satuan angstrom), jari-jari atom Be adalah …
(A) 0,80
(B) 0,89
(C) 1,23
(D) 1,57
(E) 2,03
Jawaban: B
Jari-jari atom dalam satu golongan dari atas ke bawah makin besar
Sedangkan dalam satu periode dari kiri ke kanan makin kecil
Urutan jari-jari atom dari yang terbesar hingga terkecil adalah:
K = 2,01, Na = 1,57, Li = 1,23, Be = 0,89, B = 0,80
Soal 14
Diketahui beberapa unsur dengan konfigurasi elektron sebagai berikut:
P : 2, 8, 1
Q : 2, 8, 4
R : 2, 8, 7
S : 2, 8, 8
T : 2, 8, 8, 1
Unsur yang mempunyai keelektronegatifan terbesar adalah …
(A) P
(B) Q
(C) R
(D) S
(E) T
Jawaban: C
Unsur yang memiliki nilai keelektronegatifan terbesar adalah R karena terletak di golongan VIIA
Soal 15
Manakah senyawa yang memiliki bentuk molekul linear?
(A) \(\ce {CO2}\)
(B) \(\ce {H2O}\)
(C) \(\ce {CCl4}\)
(D) \(\ce {BCl3}\)
(E) \(\ce {SF6}\)
Jawaban: A
Bentuk molekul setiap senyawa:
\(\ce {CO2} : \text{ linear}\)
\(\ce {H2O} : \text{ menyudut/bentuk V}\)
\(\ce {CCl4} : \text{ tetrahedral}\)
\(\ce {BCl3} : \text{ segitiga datar}\)
\(\ce {SF6} : \text{ oktahedral}\)
Soal 16
Diketahui unsur \(\ce {A}\) dengan nomor atom 15 berikatan kimia dengan unsur \( \ce {B}\) dengan nomor atom 17 membentuk senyawa \(\ce {AB3}\). Bentuk molekul senyawa \(\ce {AB3}\) adalah …
(A) Segitiga datar
(B) Tetrahedral
(C) Piramida trigonal
(D) Bipiramida trigonal
(E) Jungkat-jungkit
Jawaban: C
Unsur A terletak pada golongan VA, sehingga memiliki 5 elektron valensi
Unsur B terletak pada golongan VIIA, sehingga memiliki 7 elektron valensi
Karena pada atom pusat A terdapat 3 pasang elektron ikatan (PEI) dan 1 pasang elektron bebas (PEB) maka tipe molekul \(\ce {AB3}\) adalah \(\ce {AX3E}\). Bentuk molekul \(\ce {AB3}\) adalah piramida trigononal.
Soal 17
Bentuk molekul \(\ce {SF4}\) adalah …
(A) Linear
(B) Segitiga datar
(C) Tetrahedral
(D) Jungkat-jungkit
(E) Bipiramida trigonal
Jawaban: D
Pada atom pusat \(\ce {S}\) terdapat 4 PEI (pasangan elektron ikatan) dan 1 PEB (pasangan elektron bebas), sehingga tipe molekul \(\ce {SF4}\) adalah \(\ce {AX4E}\). Bentuk molekul \(\ce {SF4}\) adalah jungkat-jungkit.
Soal 18
Gaya antar molekul yang paling lemah terdapat pada interaksi antar senyawa …
(A) \(\ce {CH4}\)
(B) \(\ce {HCl}\)
(C) \(\ce {H2O}\)
(D) \(\ce {KCl}\)
(E) \(\ce {NH3}\)
Jawaban: A
Gaya antar molekul yang paling lemah adalah gaya london (gaya dispersi). Gaya london dapat terjadi antar molekul nonpolar, misalnya \(\ce {CH4}\)
Soal 19
Terdapat beberapa senyawa:
- etanol
- air
- hidrogen fluorida
- metana
- aseton
Senyawa yang memiliki titik didih paling tinggi adalah …
(A) etanol
(B) air
(C) hidrogen fluorida
(D) metana
(E) aseton
Jawaban: B
Antar molekul air terdapat ikatan hidrogen yang kuat, sehingga air memiliki titik didih yang tinggi.
Soal 20
Xenon tergolong dalam gas mulia dapat berikatan dengan unsur Fluorin yang memiliki nilai keelektronegatifan yang tinggi membentuk senyawa \(\ce {XeF4}\).
Tipe hibridisasi \(\ce {XeF4}\) adalah … (diketahui nomor atom \(\ce {Xe} = 54\), dan nomor atom \(\ce {F} = 9\))
(A) sp
(B) sp²
(C) sp³
(D) sp³d
(E) sp³d²
Jawaban: E
